4. Ünite: Saf Madde ve Karışımlar Konu Anlatımı
1.Bölüm: Maddenin Tanecikli Yapısı
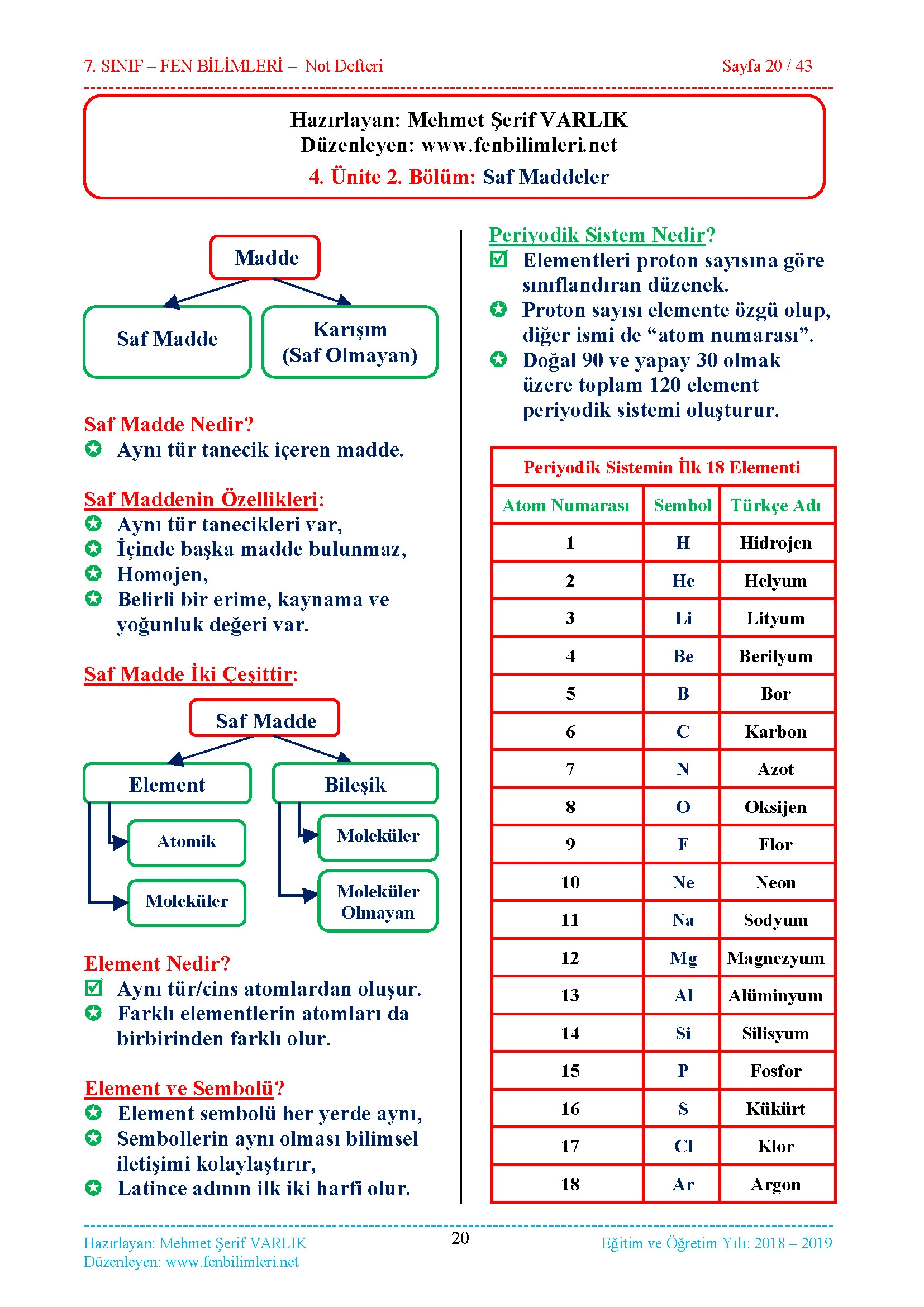
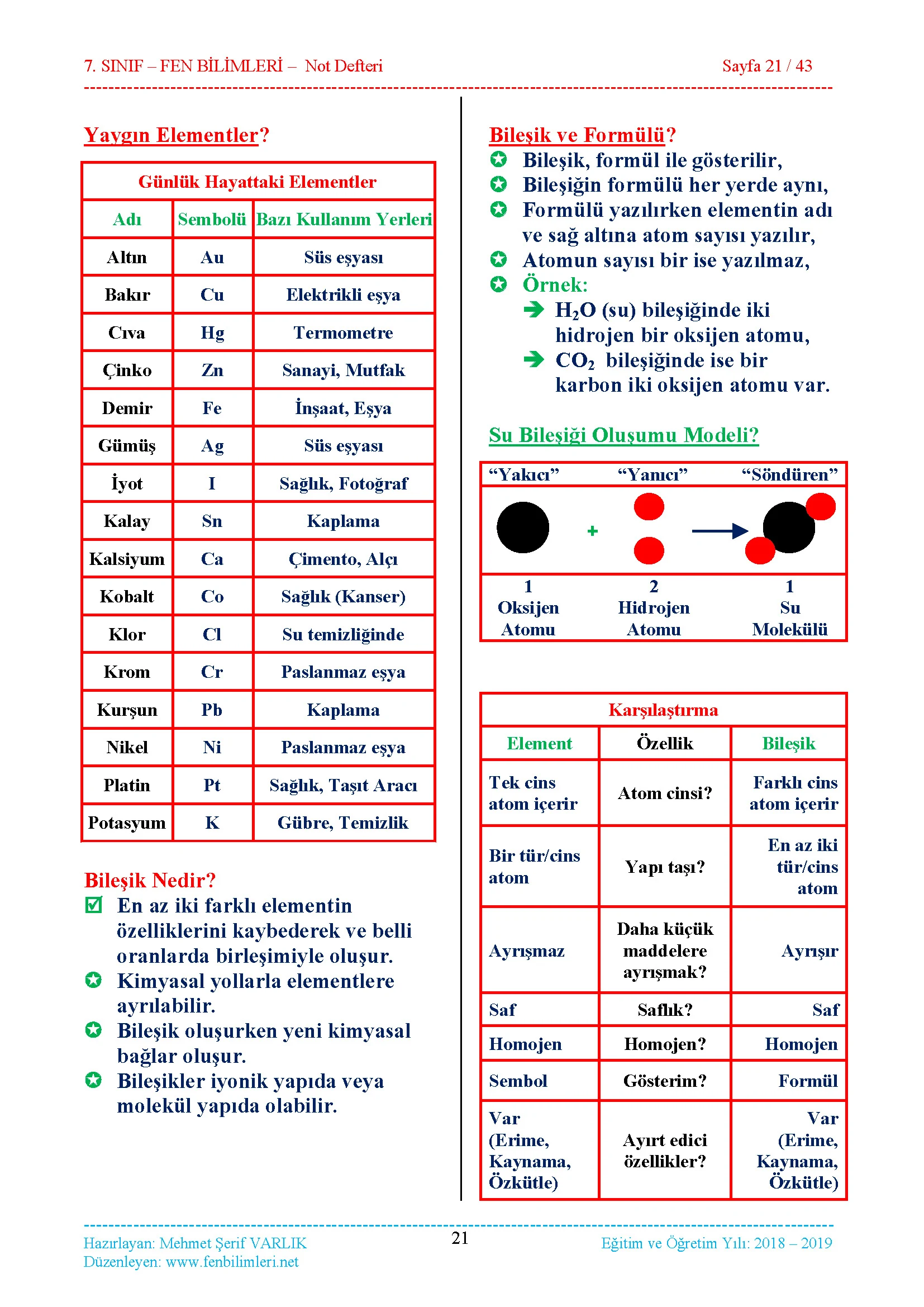
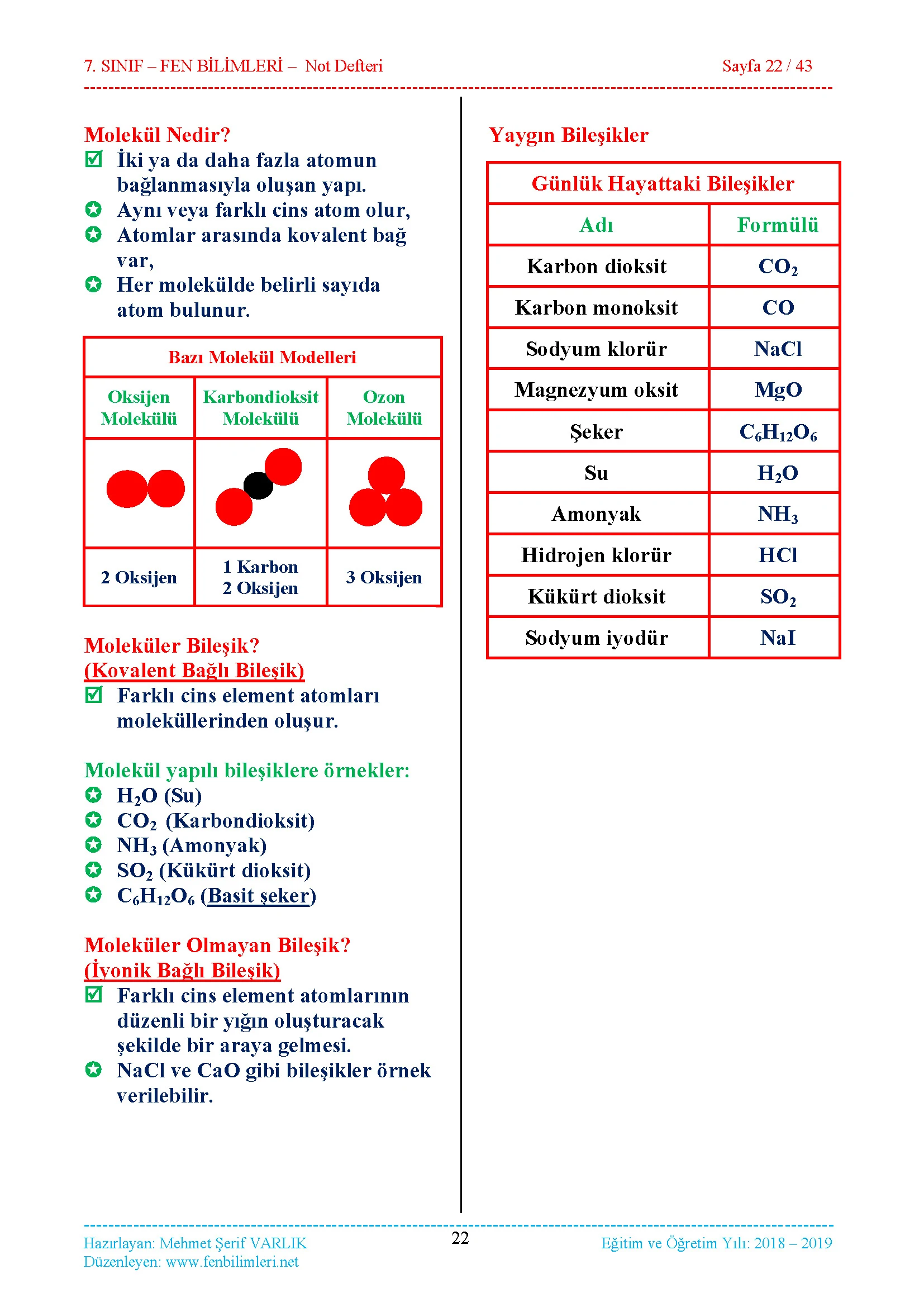
2.Bölüm: Saf Maddeler
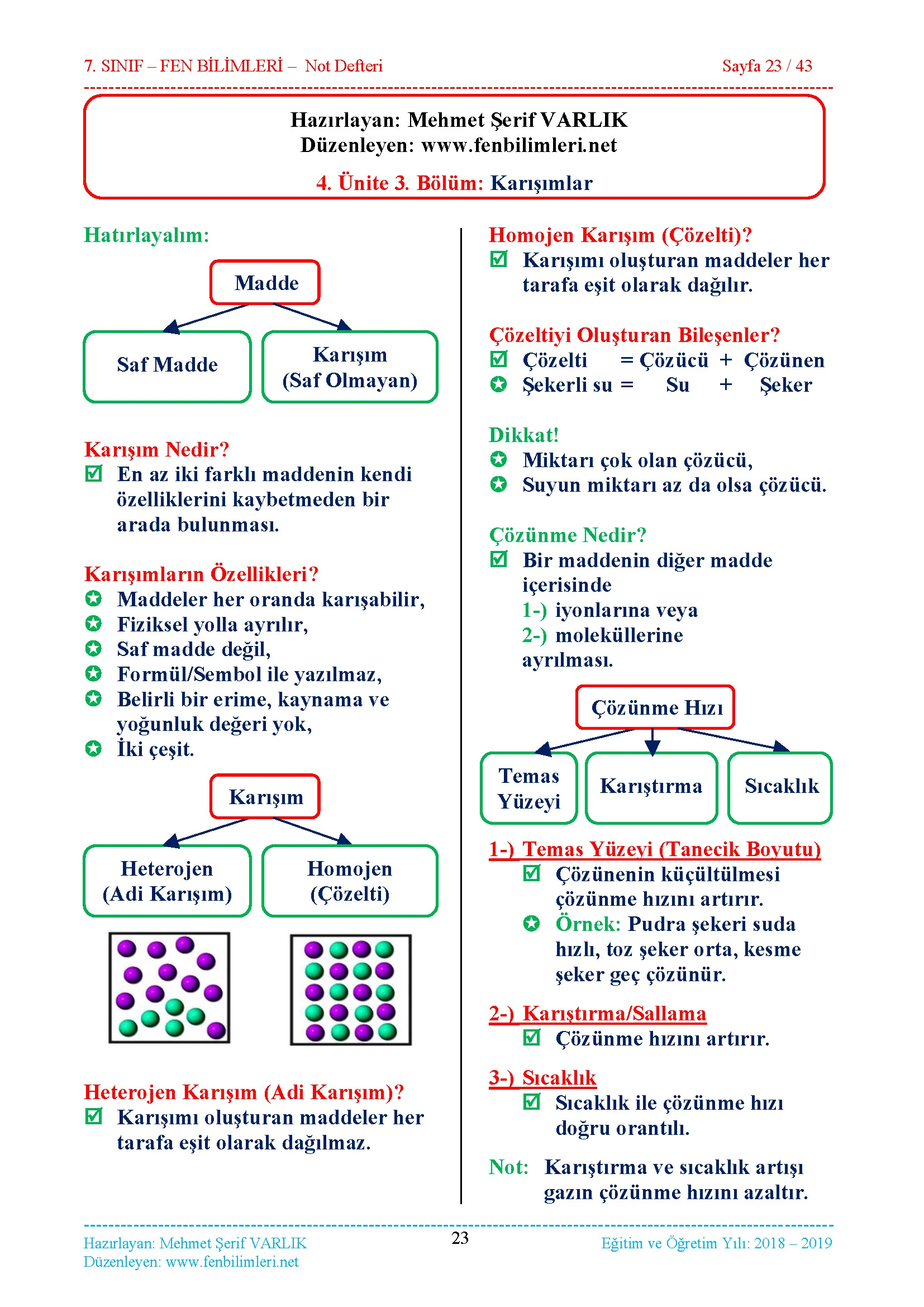
3.Bölüm: Karışımlar
4.Bölüm: Karışımların Ayrılması
5.Bölüm: Evsel Atıklar ve Geri Dönüşüm
Etiketler :
7-sinif-konu-anlatimi









Teşekkürler. İyi çalışmalar :)
YanıtlaSil